Kalsiyum karbonat tepkimesi nedir ve nasıl gerçekleşir?
Kalsiyum karbonat tepkimesi, doğal ve endüstriyel süreçlerde önemli bir rol oynayan bir kimyasal reaksiyondur. Asitlerle etkileşime girdiğinde karbondioksit ve kalsiyum tuzları üreterek çeşitli uygulamalara zemin hazırlar. Bu süreç, çevresel denge ve endüstriyel üretim açısından kritik öneme sahiptir.
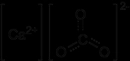
Kalsiyum Karbonat Tepkimesi Nedir ve Nasıl Gerçekleşir?Kalsiyum karbonat (CaCO₃), doğada yaygın olarak bulunan bir bileşiktir ve özellikle kireçtaşı, mermer ve kalsit gibi minerallerde bulunur. Kalsiyum karbonatın tepkimeleri, özellikle asitlerle gerçekleştirdiği reaksiyonlarla bilinir ve bu reaksiyonlar birçok endüstriyel ve doğal süreçte önemli rol oynamaktadır. Kalsiyum Karbonatın Kimyasal Formülü Kalsiyum karbonatın kimyasal formülü CaCO₃'tır. Bu bileşen, bir kalsiyum atomu (Ca), bir karbon atomu (C) ve üç oksijen atomundan (O) oluşur. Kalsiyum karbonat, hem inorganik hem de organik kaynaklarda bulunabilir ve birçok farklı formda (örneğin, kalsit, aragonit) varlık gösterir. Kalsiyum Karbonat Tepkimesinin Özellikleri Kalsiyum karbonat, çeşitli kimyasal tepkimelere girebilir. Bu tepkimelerin en yaygını, asitlerle gerçekleştirdiği tepkimelerdir. Kalsiyum karbonat, asidik bir ortamda karbondioksit (CO₂), su (H₂O) ve kalsiyum tuzları üretir. Bu tepkimenin genel denklemi aşağıdaki gibidir:
Bu tepkimede kalsiyum karbonat, hidroklorik asit (HCl) ile reaksiyona girerek kalsiyum klorür (CaCl₂), karbondioksit gazı (CO₂) ve su (H₂O) üretir. Kalsiyum Karbonat Tepkimesinin Uygulamaları Kalsiyum karbonat tepkimeleri, birçok endüstri ve bilimsel alanda önemli uygulamalara sahiptir. Bu uygulamalardan bazıları şunlardır:
Kalsiyum Karbonatın Fiziksel ve Kimyasal Özellikleri Kalsiyum karbonat, beyaz, kristal yapıda bir katıdır. CaCO₃'nin fiziksel ve kimyasal özellikleri şu şekildedir:
Kalsiyum Karbonat Tepkimesinin Çevresel Etkileri Kalsiyum karbonatın çevresel etkileri, doğada karbon döngüsünde önemli bir rol oynamasından kaynaklanmaktadır. Kalsiyum karbonatın çözünmesi, karbondioksit salınımına neden olur ve bu da iklim değişikliği üzerinde etkilidir. Ayrıca, kalsiyum karbonatın kullanımı su kaynaklarının asidikleşmesini önleyebilir. Sonuç Kalsiyum karbonat, hem doğal hem de endüstriyel süreçlerde önemli bir bileşiktir. Tepkimesi, asidik ortamlarda karbondioksit ve kalsiyum tuzları üretir. Bu tepkimeler, inşaat, gıda, kimya ve çevre bilimlerinde birçok uygulama alanına sahiptir. Kalsiyum karbonatın hem fiziksel hem de kimyasal özellikleri, onun çeşitli endüstriyel süreçlerde kullanılmasını mümkün kılmaktadır. |





.webp)