
Kalsiyum Oksit Özellikleri ve Faydaları Nelerdir?
Kalsiyum oksit (CaO), birçok endüstriyel ve tarımsal alanda önemli bir bileşiktir. Bu yazıda, kalsiyum oksitin fiziksel ve kimyasal özellikleri, faydaları ve kullanım alanları detaylı bir şekilde incelenecektir. Ayrıca sağlık üzerindeki etkileri de ele alınacaktır.
Kalsiyum oksit (CaO), kalsiyum ve oksijen elementlerinin bileşiği olan inorganik bir kimyasaldır. Genellikle "kireç" olarak adlandırılır ve birçok endüstriyel uygulama ve bilimsel araştırmalarda önemli bir rol oynamaktadır. Bu yazıda, kalsiyum oksitin özellikleri, faydaları ve kullanım alanları detaylı bir şekilde ele alınacaktır. Kalsiyum Oksitin Fiziksel ve Kimyasal Özellikleri Kalsiyum oksit, beyaz renkte, toz halinde bir madde olup, su ile reaksiyona girdiğinde kalsiyum hidroksit (Ca(OH)₂) oluşturur. Aşağıda kalsiyum oksitin bazı temel özellikleri listelenmiştir:
Kalsiyum Oksitin Faydaları ve Kullanım Alanları Kalsiyum oksit, birçok endüstriyel ve tarımsal alanda çeşitli faydalar sağlamaktadır. Aşağıda bu faydalara ve kullanım alanlarına değinilmiştir:
Kalsiyum Oksitin Sağlık Üzerindeki Etkileri Kalsiyum oksit, bazı sağlık yararlarına sahip olmasına rağmen, dikkatli kullanılmadığında zararlı etkileri olabilir. Aşağıda bu konuda bazı bilgiler verilmiştir:
Sonuç Kalsiyum oksit, çeşitli endüstriyel ve tarımsal uygulamalarda önemli bir bileşen olarak karşımıza çıkmaktadır. Fiziksel ve kimyasal özellikleri, bu bileşiğin çok yönlü kullanımını mümkün kılmakta ve sağladığı faydalar, hem ekonomik hem de çevresel açıdan değerlidir. Ancak, sağlık üzerinde olumsuz etkiler yaratmaması için dikkatli ve bilinçli bir şekilde kullanılması gerekmektedir. Kalsiyum oksitin potansiyel yararları ve uygulama alanları, gelecekte daha fazla araştırma ve geliştirme ile daha da genişleyebilir. Ek olarak, kalsiyum oksit ile ilgili yapılan araştırmalar, bu bileşiğin çevresel sürdürülebilirlik açısından da önemli fırsatlar sunduğunu göstermektedir. Özellikle, atık yönetimi ve yenilenebilir enerji alanlarında kalsiyum oksit kullanımı üzerinde çalışmalar devam etmektedir. Bu bağlamda, kalsiyum oksitin potansiyeli, bilim ve sanayi alanında önemli bir araştırma konusu olmaya devam etmektedir. |






.webp)




















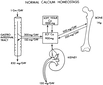




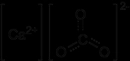







Sönmemiş kireç nedir? Kalsiyum oksit olarak bilinen bu madde, inşaat sektöründe ve tarımda yaygın olarak kullanılır. Su ile birleştiğinde kalsiyum hidroksit oluşturur. Ancak dikkatli kullanılmazsa ciltte tahrişe neden olabilir. Bu nedenle koruyucu ekipman kullanmak önemlidir.
Sönmemiş Kireç Nedir?
Berşe, sönmemiş kireç, kalsiyum oksit olarak bilinen bir kimyasal bileşiktir. İnşaat sektöründe, özellikle beton yapımında, harçların ve sıvaların hazırlanmasında önemli bir rol oynar. Ayrıca tarımda da toprak düzenleyici olarak kullanılır.
Su ile Etkileşimi
Sönmemiş kireç, su ile birleştiğinde kalsiyum hidroksit oluşturur. Bu reaksiyon, ısınma ile birlikte gerçekleştiği için dikkatli olmak gerekir. Kalsiyum hidroksit, çeşitli uygulamalarda kullanılsa da, sönmemiş kireç ile çalışırken dikkatli olunmalıdır.
Güvenlik Önlemleri
Ciltle teması tahrişe yol açabileceğinden, koruyucu ekipman kullanmak oldukça önemlidir. Koruyucu eldivenler ve gözlükler, olası yaralanmaları önlemek için önerilmektedir. Bu nedenle, sönmemiş kireç ile çalışırken dikkatli olmak ve uygun güvenlik önlemlerini almak gerekmektedir.
Sönmemiş kireç hakkında daha fazla bilgi edinmek istiyorum. Özellikle kalsiyum oksit (CaO) ile ilgili uygulamalarının detayları nelerdir? Sönmemiş kireç formülü ile ilgili örnekler verebilir misiniz? Bu malzemenin endüstrideki rolü oldukça merak edici.
Sönmemiş Kireç Nedir?
Sönmemiş kireç, kalsiyum oksit (CaO) olarak bilinen bir bileşiktir ve genellikle kalsiyum karbonatın (CaCO₃) yüksek sıcaklıkta ısıtılmasıyla elde edilir. Bu işlem sırasında kalsiyum karbonat, karbondioksit (CO₂) gazını serbest bırakarak kalsiyum oksit üretir.
Kalsiyum Oksit (CaO) Uygulamaları
Kalsiyum oksit, birçok endüstriyel uygulamada önemli bir rol oynamaktadır. İşte bazı örnekler:
1. Çimento Üretimi: Kalsiyum oksit, çimento üretiminde temel bir bileşen olarak kullanılır. Sönmemiş kireç, çimento ve betonun dayanıklılığını artırır.
2. Su Arıtma: Sönmemiş kireç, su arıtma işlemlerinde pH düzeyini artırmak için kullanılır. Suya eklendiğinde, asidik bileşenleri nötralize ederek suyun kalitesini iyileştirir.
3. Metallerin İşlenmesi: Kalsiyum oksit, metalurji endüstrisinde, özellikle demir ve çelik üretiminde cüruf oluşturucu olarak kullanılır. Cüruf, metal üretiminde istenmeyen impüriteleri ayırmaya yardımcı olur.
4. Tarım: Tarımda, toprak asiditesini azaltmak ve mineral içeriğini artırmak için sönmemiş kireç uygulanır.
Sönmemiş Kireç Formülü
Sönmemiş kireç formülü, kalsiyum oksit olarak CaO şeklinde ifade edilir. Diğer bazı bileşenlerle birlikte kullanıldığında, örneğin:
- CaO + H₂O → Ca(OH)₂ (Kalsiyum hidroksit)
- CaO + CO₂ → CaCO₃ (Kalsiyum karbonat)
Bu reaksiyonlar, sönmemiş kirecin su ile tepkimeye girdiğinde kalsiyum hidroksit oluşturması veya karbondioksit ile tepki vererek kalsiyum karbonat oluşturması gibi durumları içermektedir.
Sonuç olarak, Alemdar Bey, sönmemiş kireç ve kalsiyum oksit, endüstride çok yönlü bir malzeme olarak önemli bir yer tutmakta ve çeşitli alanlarda kullanılmaktadır. Bu malzemenin birçok endüstriyel süreçteki rolü, onun değerini ve önemini artırmaktadır.
Sönmemiş kireç kullanırken herhangi bir koruyucu ekipman kullanmam gerekiyor mu? Beyaz renkte, aşındırıcı ve alkalik bir katı olduğunu okudum, bu yüzden cildime veya gözlerime zarar verir mi? Ayrıca, kireci suyla karıştırırken dikkat etmem gereken bir şey var mı?
Merhaba Ürün,
Sönmemiş kireç kullanırken dikkatli olmanı tavsiye ederim. Bu madde, dediğin gibi alkalik ve aşındırıcı olduğu için cildine ve gözlerine zarar verebilir. Bu nedenle, koruyucu ekipman kullanman önemlidir. Aşağıda dikkat etmen gereken noktaları belirttim:
1. Eldiven Kullanımı: Kirecin cildine temasını önlemek için dayanıklı eldivenler kullanmalısın.
2. Göz Koruyucu: Gözlerine kireç kaçması durumunda ciddi zarar görülebilir. Bu nedenle koruyucu gözlük takmalısın.
3. Maske: Kireç tozu solunum yollarını tahriş edebilir. Bu nedenle bir maske kullanarak bu riskleri azaltabilirsin.
4. Su ile Karıştırma: Kireci suyla karıştırırken dikkatli ol. Kirecin suya eklendiğinde çok fazla sıcaklık oluşabilir ve bu durum yanıklara sebep olabilir. Yavaş ve kontrollü bir şekilde ekleme yapmalısın.
Bu önlemleri aldığın takdirde sönmemiş kireçle çalışırken daha güvende olursun. Dikkatli çalışmanı tavsiye ederim.