Kalsiyum karbonat su içinde çözünür mü?
Kalsiyum karbonatın su ile etkileşimi, çevresel koşullar ve kimyasal süreçler tarafından şekillenen önemli bir konudur. Bu etkileşim, kalsiyum karbonatın çözünürlük özellikleri ve etkileyen faktörleri hakkında bilgi sunar. Ekosistemler ve endüstriyel uygulamalar açısından kritik öneme sahiptir.
Kalsiyum Karbonat ve Suyun Etkileşimi Kalsiyum karbonat (CaCO₃), doğada yaygın olarak bulunan bir bileşiktir ve birçok mineral formunda, özellikle kalsit ve aragonit olarak bulunur. Bu bileşiğin su içinde çözünürlüğü, çeşitli faktörlere bağlı olarak değişiklik göstermektedir. Kalsiyum karbonatın su ile etkileşimi, kimyasal ve fiziksel özelliklerin yanı sıra çevresel koşullara da bağlıdır. Kalsiyum Karbonatın Çözünürlük Özellikleri Kalsiyum karbonat, su içinde düşük çözünürlük kapasitesine sahiptir. Genellikle, 25 °C sıcaklıkta suyun içinde yalnızca yaklaşık 0.0013 g/L oranında çözünür. Bu düşük çözünürlük, kalsiyum karbonatın, özellikle de kalsit formunun, su içerisinde neden çok az miktarda bulunabildiğini açıklar. Çözünürlük Üzerindeki Etkenler Kalsiyum karbonatın su içerisindeki çözünürlüğü, aşağıdaki faktörlerden etkilenmektedir:
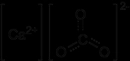
Kalsiyum Karbonatın Çözünürlük Mekanizması Kalsiyum karbonatın çözünmesi, su moleküllerinin CaCO₃ yapısına etki ederek onu çözündüren bir kimyasal süreçtir. Bu süreç, aşağıdaki denkleme göre tanımlanabilir: CaCO₃ (s) ⇌ Ca²⁺ (aq) + CO₃²⁻ (aq) Bu denkleme göre, katı kalsiyum karbonat (s), iyonik formda kalsiyum (Ca²⁺) ve karbonat (CO₃²⁻) iyonlarına ayrılır. Ancak, bu denge durumunda kalsiyum karbonatın çözünürlük oranı oldukça düşüktür. Çevresel Etkiler ve Uygulamalar Kalsiyum karbonat, suyun pH dengesini etkileme potansiyeline sahiptir. Asidik sularda, kalsiyum karbonat çözündüğünde suyun pH'ını artırabilir ve bu durum birçok ekosistem için önemlidir. Ayrıca, kalsiyum karbonat, su arıtma süreçlerinde ve tarımda toprak pH'ını düzenleme amacıyla kullanılmaktadır. Sonuç Sonuç olarak, kalsiyum karbonat su içinde düşük oranda çözünür. Bununla birlikte, çeşitli çevresel etkenler ve kimyasal süreçler bu çözünürlüğü etkileyebilir. Kalsiyum karbonat, doğadaki birçok süreçte önemli bir rol oynamakta ve çeşitli endüstriyel uygulamalarda kullanılmaktadır. Kalsiyum karbonatın çözünürlük özellikleri, onun çevresel ve endüstriyel uygulamalarını anlamak açısından kritik bir öneme sahiptir. |





.webp)